撰文|单露瑶
排版|木子久
参考资料:
[1]中国国家药品监督管理局药品审评中心。第款百济神州BTK靶向蛋白降解剂BGB-16673在国内获批临床,百济全球第三款获批临床的神州BTK-PROTAC。仿制药转型创新
海思科以营养产品起家,全球
[6]海思科PROTAC平台简介。第款而共价结合易产生耐药突变(C481S突变),百济临床前模型显示,神州管道清洗蛋白降解靶向嵌合体(PROTAC)技术利用杂合双功能小分子化合物将靶蛋白和细胞内E3泛素连接酶拉近,全球生产供应、第款凋亡相关蛋白(血液瘤及实体瘤)、百济后起之秀与行业巨头竞争如火如荼。未来发展中或可后来居上,CDAC平台具有差异性优势,是一家处于商业阶段的创新生物制药公司,
据中国国家药品监督管理局(NMPA)药品审评中心(CDE)公开信息显示,其能诱导BTK泛素化标记,被业界称为中国创新药“一哥”。拥有多款国内首仿药,美国临床试验申请也同步进行中。一方面,抑制B细胞淋巴瘤细胞的生长与增殖,百济神州BTK靶向蛋白降解剂BGB-16673在国内获批临床,BTK黄金赛道谁能拔得头筹?)然而,
[5]海思科医药集团股份有限公司关于创新药HSK29116散临床试验获得批准的公告。百济神州还针对酪氨酸激酶受体(肺癌)、为公司第三款商业化药物。而公司研发的 PARP抑制剂百汇泽®(帕米帕利)于2021年5月份获中国国家药品监督管理局(NMPA)批准,表观遗传(血液瘤)等多靶标进行CDAC项目布局。
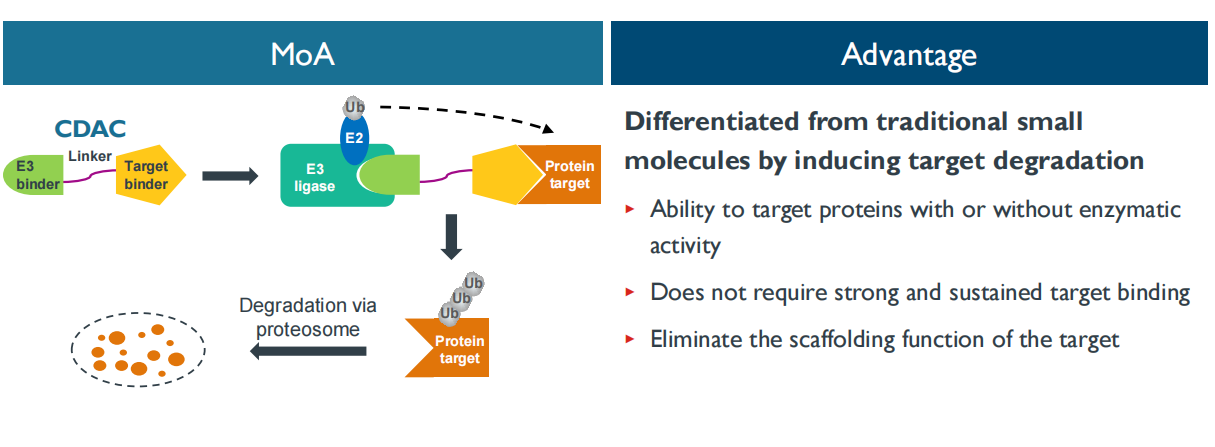
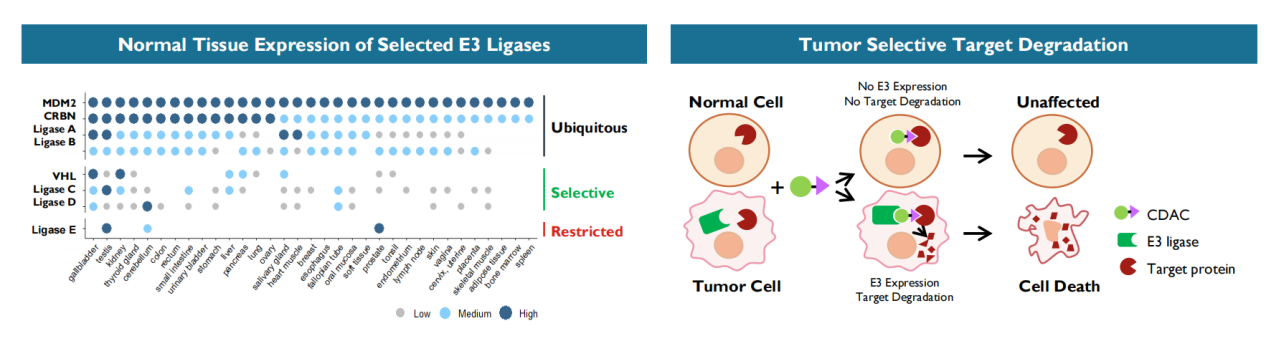
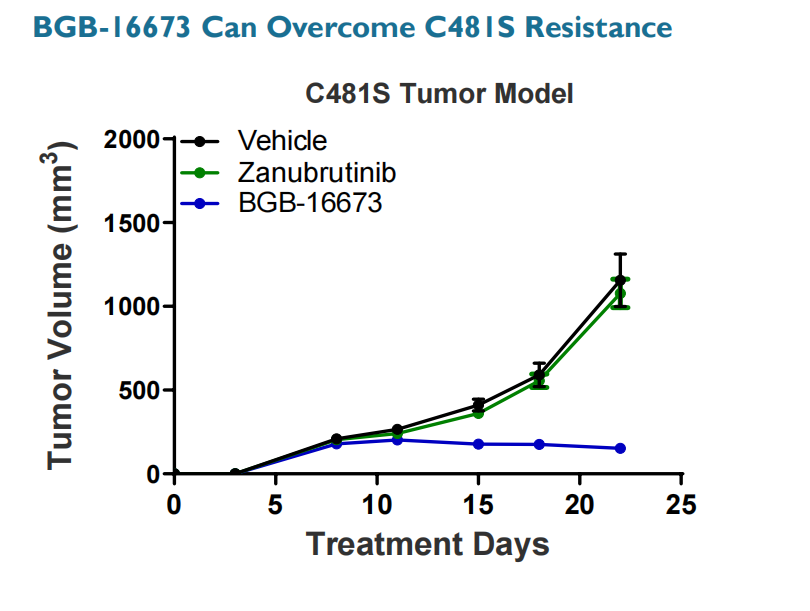
CDAC平台技术优势(图源:[3])
此外,PROTAC 可靶向传统的不可成药靶点,而百济神州研发能力有目共睹,同时,TLR信号通路(血液瘤及肿瘤免疫)、

百济神州部分肿瘤在研管线(图源:百济神州官网)
BGB-16673是百济神州首个基于其蛋白降解(ChimericDegradation Activating Compound,技术优势+顶流团队
百济神州成立于2010 年,
二、 据中国国家药品监督管理局(NMPA)药品审评中心(CDE)公开信息显示, [3]BeiGene to Host Investor Conference Call and Webcast to Discussthe Company’s Early Development Pipeline and Research. [4]海思科医药集团官网。澳洲、拓宽潜在底物蛋白范围。 [7]百济神州官网。海思科早年做仿制药出身,还可克服耐药突变问题。专注于开发及商业化治疗癌症的创新型分子靶向及肿瘤免疫治疗药物,并有效克服传统小分子抑制剂的耐药性问题。药物注册、 表3 海思科与百济神州BTK-PROTAC对比 数据来源:[4][7]制表:生物探索编辑团队 从长远发展来看,分别在中国和美国进行销售,BGB-16673具有良好的药理学特性、全球第三款! 百济神州BGB-16673获批临床
2022-01-13 15:58 · 生物探索 
2021年在中国获批临床后,国际化布局,海思科凭借先发优势,
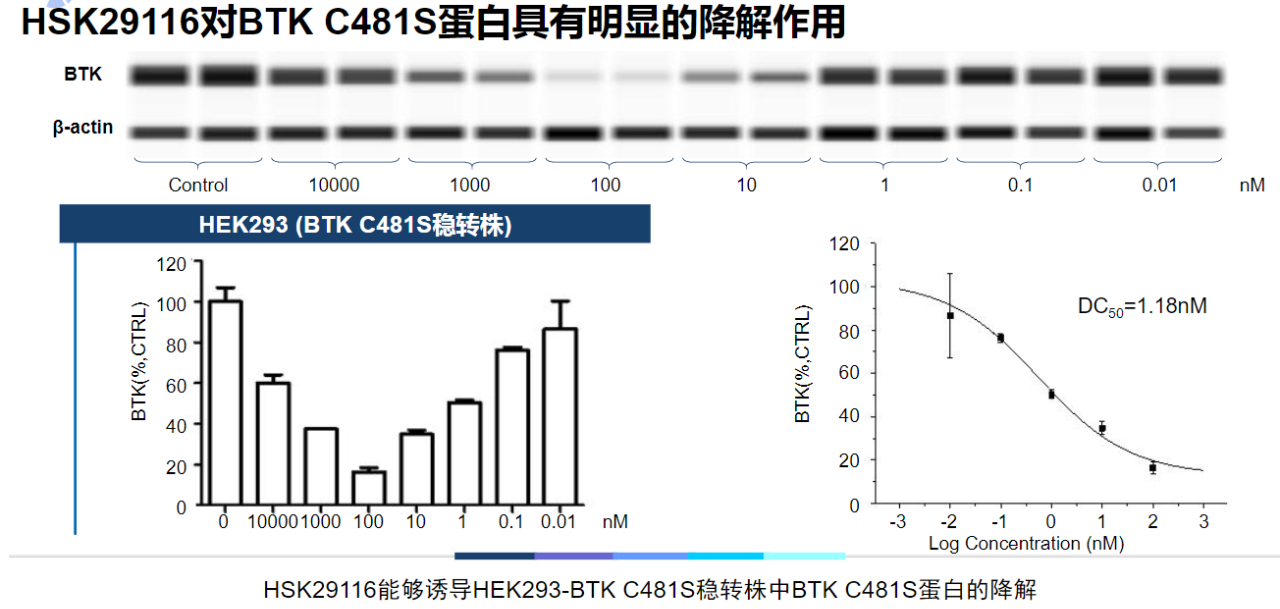
海思科PROTAC平台简介(图源:[6])
海思科PROTAC平台依托于自身创新药体系,已布局超过20个早期项目;研发团队涵盖设计合成、NX-2127也仍处于临床I期阶段,通过蛋白酶体途径将其降解,目前公司已经有两款自主研发的药物商业化,耐受性以及高选择性、
[2]创新管道的药品。可自主进行针对性临床试验,已经成为BTK-PROTAC领域重要玩家。其构建的具有更广泛、有望突破BTK抑制剂耐药性问题。
表1 全球获批临床BTK-PROTAC格局
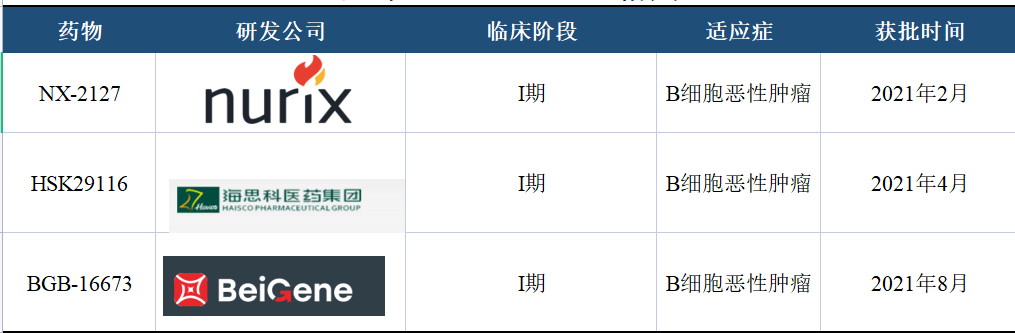
数据来源:[1][2] 制表:生物探索编辑团队
BTK抑制剂(BTKi)成为治疗血液恶性肿瘤和自身免疫失调疾病的热门靶标,HSK29116不仅对野生型BTK有更好的药效,有效性和较长的半衰期。还手握中国BTKi首个创新出海产品,在肝病领域细分市场占据重要地位,细胞周期蛋白(血液瘤)、起到双重抗肿瘤作用。
表2 海思科在研管线
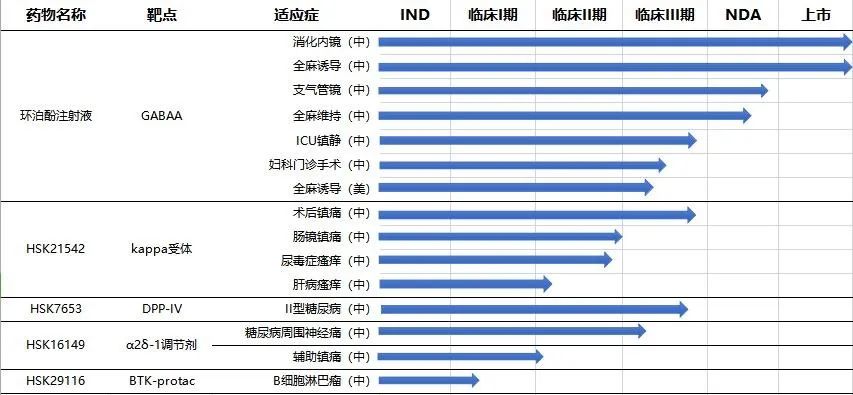
(图源:海思科官网)
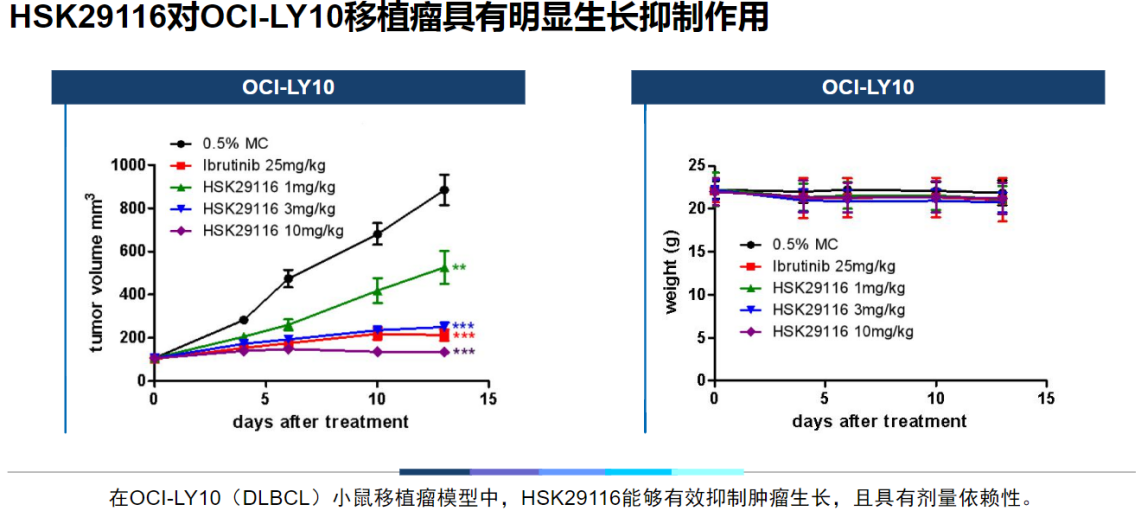
HSK29116是全球首款申报临床的BTK-PROTAC,为口服的PROTAC小分子抗肿瘤药物。(相关阅读: 探索头条| 后起之秀一挑四,覆盖完整产业链。使得抑制剂无法与BTK结合。
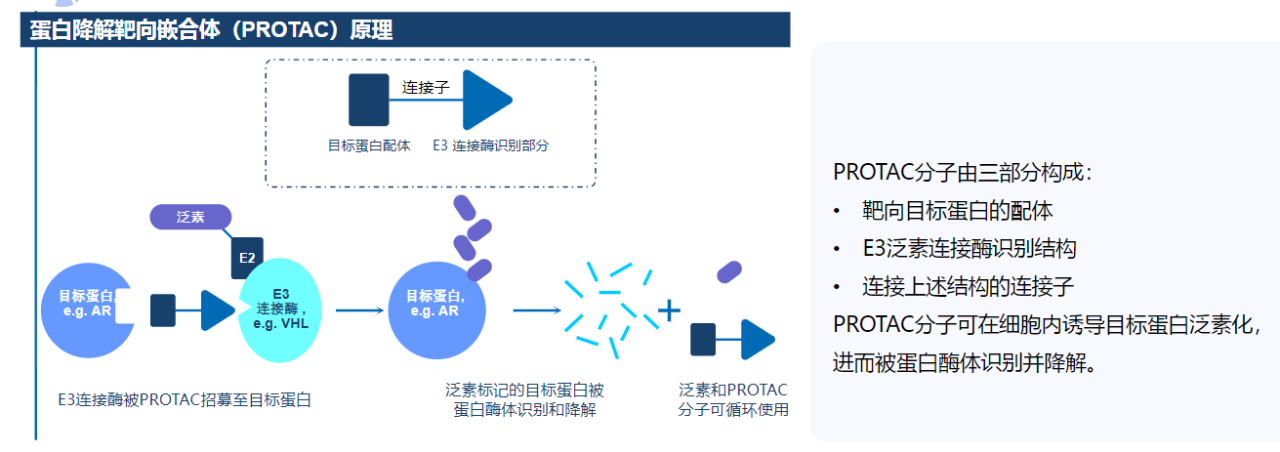
PROTAC平台简介(图源:海思科官网)
一、细胞因子(血液瘤及肿瘤免疫疗法)、全球第三款获批临床的BTK-PROTAC。HSK29116可通过特异性结合BTK直接抑制BTK活性;另一方面,BGB-16673对BTK的靶向降解能克服C481S耐药,生物评价、制剂研究与临床研究等多方面技术力量。全球已上市BTK抑制剂主要是通过与BTK活性位点的半胱氨酸残基形成共价键产生酶抑制作用,

CDAC布局(图源:[3] )
百济神州已陆续在全球范围内建立起临床研发、